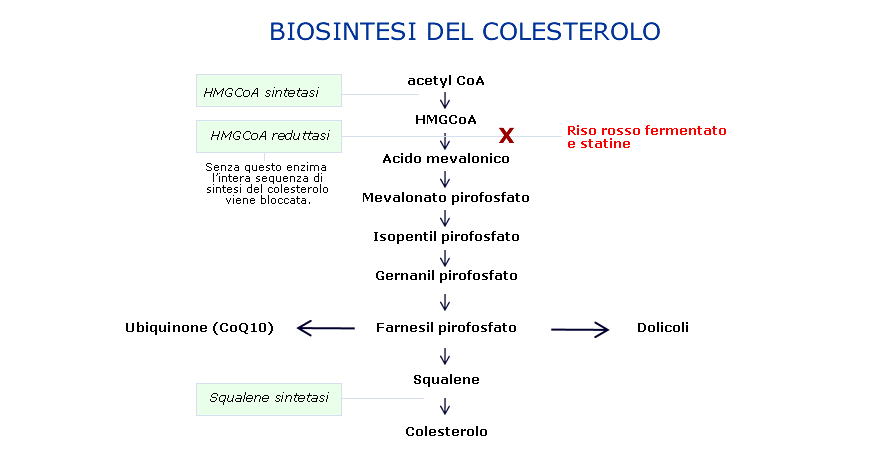
Il Monascus purpureus è un fungo tradizionalmente impiegato in Cina da millenni per la produzione del vino di riso. Si tratta in realtà di una microrganismo di tipo sferico (dimensioni medie 5μ di diametro) o ovoide (5×6 μ M). All’inizio il micelio è bianco , comunque diventa rapidamente rosa prima e arancione-rosso poi, riflettendo l’aumentata acidità nel medium. Il Monascus causa fermentazione della cellulosa, del maltosio, fruttosio e glucosio ma non fermenta la canna da zucchero (Yin et al 1987). Tradizionalmente il fungo viene utilizzato per fermentare una cottura non glutinosa di riso, con un’erba del genere Polygonum, secondo una millenaria ricetta tradizionale per produrre il famoso vino rosso di riso. In realtà il processo d fermentazione è dovuto a due microrganismi, il fungo, Monascus purpureus, è una muffa, il primo in grado di degradare l’amido in semplici zuccheri, mentre la seconda rende possibile la conversione in alcool. Il fungo di fatto veniva tradizionalmente coltivato sul riso ed era il rapido sviluppo del micelio con i suoi pigmenti rossi che finiva con il permeare completamente i grani di riso conferendo il tipo colore rosso (Sung 1966). L’impiego del fungo può essere fatto risalire quanto meno alla dinastia Tang. (800 A.D). L’antica farmacopea cinese , Ben Cao Gang Mu-Dan Shi Bin Yi, pubblicata durante la dinastia Ming (1368-1644) contiene una descriozine dettagliata della preparazione di prodotti alimentari a medicinali a base di Monascus (Sung 1966). Le sue principali indicazioni tradizionali sono costituite dai disturbi dovuti all’accumulo di grassi (nosologicamente riconducibili ai problemi di stasi di circolo nella Medicina Tradizionale Cinese), dai disturbi epatici , da alcune forme di tumore e dal miglioramento della circolazione sanguigna. Oggi il fungo è impiegato ampiamente in Cina, come rimedio tradizionale principalmente per i disturbi dislipidemici e in Occidente soprattutto come pigmento per carni, pesce, formaggi e bevande alcoliche e recentemente nei salumi (Oatakova-JUzlova et al 1998)
Il Monascus purpureus contiene una ampia varietà di sostanze. Sono stati descritti:
Per molti anni il Monascus purpureus divenne una delle fonti di statine e a tale scopo si sviluppò una tecnologia di coltivazione in vitro tuttora in uso (Chang et al 2002).
In realtà parlare di composti presenti nel Monascus purpureus è una questione aperta: proprio le tecniche di coltivazione in vitro hanno infatti permesso, modificando la composizione del medium dove viene coltivato il fungo, di alterare profondamente la sua composizione e probabilmente sono alla base degli sviluppi più interessanti e attuali della ricerca su questo fungo. Modificando il medium è possibile modificare la composizione del fungo e selezionare ceppi che possono essere ricchi in Monakolina K e in composti secondari, normalmente trascurabili come il GABA (acido γ-amminobutittico )(Su et al 2003) o l’acetilcolina (Kohama et al 1987). In questa maniera sono stati selezionati ceppi di volta in volta a maggior attività ipoglicemizzante o ipotensiva (Hsieh e Tai 2003). Il concetto che sta alla base di tali innovazioni è che è possibile variare la composizione del fungo attraverso una variazione delle condizioni di coltivazioni aumentando e modificando i rapporti e la presenza dei vari nutrienti. In questo senso è difficile parlare di una composizione chimica del Monascus purpureus dovendo piuttosto precisare quali sono di volta in volta le condizioni di coltivazione.
In conigli alimentati con una dieta al 25% di caseina , un modello di iperlipidemia endogena, il colesterolo serico aumenta del 400% (Li et al 1998). Quando questi animali vengono trattati con estratti di Monascus prurpureus per 30 giorni manifestano una riduzione dose dipendente di colesterolo totale (TC) e colesterolo-LDL , che alla dose maggiore (800 mg/Kg) è stata rispettivamente del 59% e del 44% rispetto ai livelli pretrattamento .La riduzione in particolare del rapporto TC/HDL risultava superiore a quella ottenibile con la corrispondente dose di lovastatina. Se i conigli vengono mantenuti in una dieta ricca in caseina per 60 giorni l’aumento in colesterolo totale rasenta il 900% e quello dei trigliceridi il 300 %. L’aggiunta di estratto di Monascus purpureus per 40 giorni (400 e 800 mg/die) riduce i livelli di TC e LDL-C del 32% e 43% rispettivamente rispetto ai livelli pretrattamento. (Lin et al 1998). Kritchevsky e coll. (1998) eseguì uno studio su conigli alimentati con dieta normale e con dieta proaterogenica (2% colesterolo) I conigli venivano poi divisi in tre gruppi: no trattamento, lovastatina (2.16 mg/die) e due dosagi di estratti di Monascus purpureus (0.4 e 1.35 mg/Kg). Dopo sei mesi i livelli di colesterolo totale e trigliceridi nel gruppo alimentato con la dieta aterogenica erano aumentati del 1400% mentre il gruppo che assumeva lovastatina registrava una diminuzione del 87% e quelli che assumevano estratti di Monascus dl 36% e del 67% rispettivamente alla dose più bassa e più alta. Wang e coll. (2000) considerarono invece un gruppo di ratti ipertrigliceridemia preparati con una dieta ricca in fruttosio(30%). Un gruppo veniva alimentato con 2% di estratto di Monascus ed uno con 250 mg/Kg di 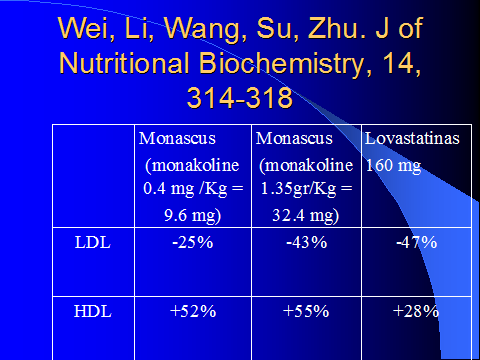 lovastatina mentre un gruppo alimentato solamente con fruttosio al 30% serviva da controllo. Il gruppo che assumeva l’estratto di Monascus purpureus manifestava un effetto ipotrigliceridemizzante ma non il gruppo che assumeva lovastatina. Questo studio era il primo che evidenziava un’azione sul metabolismo lipidico da parte degli estratti di Monascus non riconducibile all’azione della sola lovastatina. Tale dato è stato successivamente confermato da un altro studio su conigli alimentati per 200 giorni con una dieta contenente lo 0.25% di colesterolo (Wei et al 2003). I conigli venivano divisi in cinque gruppi: dieta normale di controllo, gruppo di controllo in dieta aterogena e gruppi in dieta aterogena in terapia con estratto di Monascus corrispondente a 0.4 mg/Kg (lo stesso dosaggio impiegato in clinica) e a 1.35 mg/Kg di monakolina K con lovastatina a 2.36 mg/Kg ( pari al doppio della dose massima utilizzabile in clinica). I risultati evidenziarono che mentre l’azione sul colesterolo LDL era correlabile alla concentrazione di principio attivo, lovastatina quella sul colesterolo HDL era indipendente da questa risultando anche ai dosaggi inferiori di monakolina più evidente nei gruppi trattati con estratti di Monascus che con la sola lovastatina.
lovastatina mentre un gruppo alimentato solamente con fruttosio al 30% serviva da controllo. Il gruppo che assumeva l’estratto di Monascus purpureus manifestava un effetto ipotrigliceridemizzante ma non il gruppo che assumeva lovastatina. Questo studio era il primo che evidenziava un’azione sul metabolismo lipidico da parte degli estratti di Monascus non riconducibile all’azione della sola lovastatina. Tale dato è stato successivamente confermato da un altro studio su conigli alimentati per 200 giorni con una dieta contenente lo 0.25% di colesterolo (Wei et al 2003). I conigli venivano divisi in cinque gruppi: dieta normale di controllo, gruppo di controllo in dieta aterogena e gruppi in dieta aterogena in terapia con estratto di Monascus corrispondente a 0.4 mg/Kg (lo stesso dosaggio impiegato in clinica) e a 1.35 mg/Kg di monakolina K con lovastatina a 2.36 mg/Kg ( pari al doppio della dose massima utilizzabile in clinica). I risultati evidenziarono che mentre l’azione sul colesterolo LDL era correlabile alla concentrazione di principio attivo, lovastatina quella sul colesterolo HDL era indipendente da questa risultando anche ai dosaggi inferiori di monakolina più evidente nei gruppi trattati con estratti di Monascus che con la sola lovastatina.
In uno studio cinese il sangue di volontari sani è stato sottoposto a trattamento con ioni rame, un modello farmacologico, per indurre una ossidazione delle lipoproteine e bassa densità. (colesterolo-LDL). Gli estratti di Monascus puprpuersus furono aggiunti al preparato alla stessa concentrazione (5 mg/ml) all’8°, 12°, 24°. 36° e 48° ora o a concentrazione variabili (0-10 mg/ml) alla 18° ora . In entrambi gli esperimenti il Monascus purpureus dimostrò una significativa protezione rispetto alla perossidazione lipidica (Xu et al 1998).
Tali dati sono rimarchevoli in quanto l’azione antiossidante risulta più marcata di quella ottenibile con la sola dose di lovastatina corrispondente. In uno studio su 30 ratti alimentati con una dieta ricca in colesterolo inoltre la somministrazione di estratto di Monascus purpureus è stata in grado di inibire la proliferazione dell’intima delle arterie coronariche e l’espressione della proteina C Reattiva e della proteina C-myc sia rispetto al gruppo controllo sottoposto alla stessa dieta che al gruppo controllo non sottoposto a dieta iperlipidemica (Qi et al 1999).
Gli studi clinici realizzati sugli estratti di Monascus purpereus si dividono in due grandi categorie: quelli realizzati negli Stati Uniti e quelli realizzati in Cina. Diversa la filosofia. Negli Stati Uniti sono stati realizzati due studi importanti su un preparato standardizzato allo 0.4% in monakolina venduto come integratore alimentare (libera vendita) per la prevenzione delle dislipidemie, il famoso Cholestin. Si trattava quindi, per lo meno teoricamente, di un uso essenzialmente non terapeutico per soggetti per i quali non era indicata una reale terapia ipocolesterolemizzante. Il primo studio fu realizzato da Wang e coll. (1997) su 446 soggetti di cui 324 ricevettero 600 mg di un preparato a base di Monascus purpureus standardizzato allo 0.4% in monacolina due volte al giorno per otto settimane. Gli altri 122 ricevettero invece un preparato a base di Jiaogulan (Gynnostemma penthaphyllum), scelta infelice calcolando le proprietà adattogene ma anche ipocolesterolemizzanti (Cheng 1995) di questa pianta. Dopo 8 settimane il gruppo trattato manifestava una discesa del colesterolo totale (TC) del 22.7% e del colesterolo LDL del 30.9% mentre le lipoproteine a alta densità aumentavano del 19.9% ( Wang e coll 1997). Il gruppo di controllo manifestava invece una diminuzione del TC del 7.0%, del colesterolo-LDL dell’8.3% e un innalzamento del colesterolo HDL dell’8.4%. L’abbassamento dei trigliceridi era nel gruppo trattato del 34.1% rispetto al 12.8% del gruppo trattato, valori ben superiori a quanto normalmente si può ottenere con la corrispondente dose di lovastatina (4.8 mg).
Gli elevati risultati del gruppo di controllo si riferiscono al fatto che invece di scegliere una sostanza inerte venne scelta una pianta (lo jiaogulan) che possedeva di per se un effetto ipocolesterolemizzante. Il secondo studio americano venne invece realizzato su 83 soggetti (46 uomini e 37 donne) iperlipidemici: colesterolo totale : 5.28-8.74 mmol/l (204-338 mg/dl); colesterolo-LDL: 3.31-7.16 mmol/l (128-277 mg/dl); trigliceridi: 0.62-2.78 mmol/l (55-246 mg/dl) e colesterolo-HDL: 0.78-2.46 mmol/l (30-95 mg/dl). Nessuno dei partecipanti era ovviamente in trattamento con ipocolesterolemizzanti. Ai soggetti trattati venne somministrato 2.4 g/die di estratto di Monascus purpureus ( 4 capsule da 600 mg) mentre al gruppo trattato veniva somministrata una sostanza placebo. Entrambi i gruppi seguivano una dieta con il 30% delle calorie derivate da grassi , < 10% da grassi saturi, < 300 mg di colesterolo giornaliero. I valori dei lipidi nel plasma veniva misurato alla 8°, 9°,11° e 12° settimana. I risultati di questo studio furono una diminuzione significativa ne gruppo trattato apartire dalla 8° settimana per quanto riguarda il coletsterolo totale, il colesterolo LDL e i trigliceridi non per il colesterolo HDL.
Risultati Studi di Heber e coll.(1999): 2400 mg di Monascus purpureus 0.4% vs placebo dopo 4 e 8 settimane:
Di diversa prospettiva gli studi cinesi. Si tratta di 41 studi clinici focalizzati sull’attività degli estratti di Monascus purpureus (per lo più su un preparato in commercio con il nome di Xuezhikang) sul metabolismo lipidico e glicemico. I prepararti utilizzati sono standardizzati allo 0.8% in monakoline e vengono generalmente impiegati in capsule da 300 mg 4 volte al giorno , per un totale di 9.6 mg di monakolina K. Registrati come un farmaco “tradizionale” essi vengono utilizzati per lo più su prescrizione medica. Il più noto è il Xuezhikang. In uno studio su 121 pazienti iperlipidemici questi sono stati divisi in due gruppi, uno di 91 soggetti che assumevano 4 capsule da 300 mg di estratto di monascus purpureus per 8 settimane e 1 che assumeva per 8 settimane 6 capsule di Jiaogulan. Lo studio era ovviamente di tipo osservazionale dato il differente regime terapeutico: anche in questo caso restano le perplessità di utilizzare come controllo una pianta ad azione ipocolesterolemizzante. Dopo 8 settimane il gruppo trattato presentava un innalzamento dei valori di colesterolo HDL del 12.8 % e una diminuzione dei valori di colesterolo totale (TC) , colesterolo-LDL, trigliceridi del rapporto TC/colesterolo-HDL rispettivamente del 23.7%, del 30.3%, del 31.2% e del 31.6% (Lu e coll 1997). Nessuno di questi parametri cambiò in maniera significativa nel gruppo controllo. A parte il colesterolo-HDL, in tutti gli altri parametri la differenza fu significativa. Un altro studio prendeva in esame 108 soggetti divisi in due gruppi, uno di 53 casi trattati con 4 capsule di estratto di Monascus purpureus (1200 mg/die) per 8 settimane ed un secondo gruppo di soggetti che assumevano Zocor (simvastatina 10 mg/die). Alla fine delle 8 settimane i valori di colesterolo totale, colesterolo-LDL e trigliceridi scendevano rispettivamente del 23%, del 28% e del 28.1% mentre l’HDL aumentava del 5% gruppo del Monascus. Nel gruppo trattato con Zocor i rispettivi valori scendevano invece del 23.3%, del 29.5%, del 29.5% mentre i valori del colesterolo HDL aumentavano del 12%. Nessuna differenza statisticamente significativa veniva rilevata tra i due gruppi. Calcolando che il gruppo con Monascus presentava molti meno effetti collaterali rispetto al gruppo con simvastatina gli autori suggerivano un vantaggio nell’impiego del prodotto naturale (Kuo et al. 1997). E’ inoltre disponibile uno studio su 43 soggetti anziani (60-74.5 anni, media 65 ± 5) trattati con una dose alta di estratto di Monascus (2.5 gr/die): i valori del colesterolo totale (TC), e trigliceridi risultavano diminuiti dopo 8 settimane rispettivamente del 22.1% e del 37.4% rispetto al gruppo placebo (22 soggetti). Il colesterolo-HDL aumentava nel gruppo con Monascus del 10.4% rispetto al gruppo placebo (Yu et al. 1996). Risultati analoghi furono riportati in gruppi ad alto rischio come i soggetti che avevano subito un infarto miocardio recente (36 soggetti di cui 10 con infarto anteriore del setto, 16 con esteso infarto anteriore e 8 con infarto inferiore) (Deng et al 2000) e in soggetti con insufficienza renale cronica (dialisi continua peritoneale ambulatoriale: 30 soggetti, nessun effetto avverso di rilievo) (Fu and Zhang 1998) Un altro studio analizzò l’effetto sui parametri lipidemici dell’estratto di Monascus purpureus in soggetti con diabete di tipo II. I soggetti furono divisi in due gruppi, uno che assumeva due capsule da 300 mg di estratto di Monascus ed un secondo gruppo che assumeva 2 capsule di sostanza placebo (Fang and Li 2000). Gi Autori osservavano dopo 8 settimane di trattamento oltre che ad una riduzione nel gruppo trattato del colesterolo totale (TC) e dei trigliceridi, del 27.06% e del 42.3% una diminuzione della glicemia e dell’ insulinemia a digiuno rispettivamente del 39.5% e del 33.75% e della glicemia e dell’insulinemia 2 ore dopo il pasto del 49.2% e del 55.76%. Tali risultati evidenzarono un’attività antidiabetica clinicamente significativa nel 95.9-100% dei casi. Va inoltre citato uno studio clinico osservazionale effettuato su 276 soggetti affetti da marcata steatosi epatica (diagnosticata in 28 casi con biopsia epatica e in 22 con biopsia epatica dopo colecistectomia) monitorata tramite test di funzionalità epatica e esame ultrasonografico. 78 soggetti erano dipendenti da alcohol, 48 soffrivano di epatite cronica, 24 erano diabetici e 22 affetti da colelitiasi. I soggetti assumevano due capsule da 300 mg al giorno per tre cicli di 8 settimane ciascuno. Dopo 6 mesi il colesterolo totale e i trigliceridi risultavano diminuiti rispettivamente del 25.8% e del 50.7%, mentre il colesterolo-HDL aumentava del 39.17%. I risultati dell’ecografia di controllo eseguita dopo 4 mesi riportavano anch’essi un marcato miglioramento del quadro epatico in un ampio numero di soggetti (Liu and Zhao 1999).
Partendo dalle recenti evoluzioni del concetto di aterosclerosi in Cina sono stati pubblicati recentemente alcuni studi su nuove proprietà degli estratti di Monascus purpureus. Nell’aterosclerosi i meccanismi infiammatori stanno infatti assumendo sempre maggiore importanza (Ross 1999). Viene infatti ipotizzato che specifici punti del sistema arterioso siano particolarmente vulnerabili all’infiammazione: tale vulnerabilità sarebbe dovuta a sollecitazione meccaniche combinate con la presenza di elevati livelli di colesterolo-LDL e probabilmente di Lipoproteina(a). Proprio la presenza di queste sostanze favorirebbe l’adesione di monociti e linfociti T. (Tousoulis et al 2002). Una volta instauratosi questo meccanismo i macrofagi derivati dai monociti e le cellule linfocitarie rilasciano a loro volta un’ampia gamma di sostanze chemiotattiche e chemioattive. L’endotelio diventa reattivo e ciò si manifesta con l’espressione di numerosi fattori come interleukine, fattori del complemento, tumor necrosis factor , tutte sostanze che contribuiscono con un meccanismo a cascata ad amplificare lo stato infiammatorio. L’infiammazione viene favorita e mantenuta da meccanismi ossidativi correlati in parte con l’ossidazione delle lipoproteine –LDL e in parte con meccanismi di altri tipo (rilascio di ossido nitrico, adesione leucocitaria, etc ) (Epstein 1997). Questo è il motivo per cui i parametri infiammatorio sono diventati sempre più importanti nella diagnosi dell’aterosclerosi e soprattutto n determinare quali terapie siano più efficaci (Libby and Rcker 2004). Tra questi la proteina C –reattiva è senza dubbio la più attendibile. Anche la Lipoproteina A (Lp(a), proprio per la sua similarità con il plasminogeno, probabilmente gioca un ruolo importante (Tousoulis et al. 2002) nello stabilire una connessione tra i processi infiammatori e trombosi. Un recente studio ha dimostrato come l’interazione tra Lp(a) e macrofagi coinvolge più siti d’azione che sinergizzano per raggiungere una interazione molto più attiva di quella osservata tra colesterolo LDL e plasminigeno (Poon et al. 1997) E’ probabile che proprio la via dell’attivazione della trombina possa costituire un importante mecanismo nel determinare le occlusioni spontanee delle coronarie nei soggetti aterosclerotici (Haider et al 1996). Ora gli studi a nostra disposizione rivelano che le statine pur avendo una buona attivita sulla proteina C reattiva hanno scarsa attività sul sistema delle Lipoproteina (a) (Saltissi et al. 2002) quando non inducono un vero e proprio innalzamento di questo fattore di rischio (Galetta et al 1995). Gli estratti di Moascus purpureus viceversa hanno dimostrato di essere in grado no solo di abbassare, come le statine i valori della proteina C-reattiva, ma anche quelli della Lp(a) (Liu et al 2003). Uno studio su 60 soggetti con malattia coronaria divisi in due gruppi (1200 mg estratti di Monascus purpureus contro placebo per 6 settimane, ) ha infatti dimostrato come, gli estratti di Monascus siano in grado di abbassare sensibilmente l’innalzamento di trigliceridi postprandiali , di proteina C-reattiva e di Lipoproteina(a) a digiuno e dopo pasto ricco in lipidi (800 calorie -50 gr di grassi). L’effetto del Monascus purpureus sui trigliceridi postprandiali è del resto molto più evidente di quella che ci si potrebbe attendere dalla presenza della sola presenza di lovastatina. Tutte le statine infatti tendono ad avere un effetto rilevante solamente sulle ipetrigliceridemie elevate (> 250 mg/dl) a digiuno (Stein et al 1998) Su quei soggetti che invece possiedono livelli normali a digiuno ma molto altì dopo un pasto ad alto contenuto di grassi (800 calorie, 50 gr di grassi) il loro effetto è limitato (Stein et al 1998). Il Monascus purpureus invece anche in questi soggetti dopo un apporto calorico del genere è in grado di abbassare i valori dei trigliceridi alla 2°, 4° e 6° ora rispettivamente del 32%, del 38% e del 43% (Zhao et al. 2003). Tale azione è paragonabile a quanto ottenibile solo con dosi molto più alte di statine sintetiche, corrispondenti a 40 mg di simvastatina (Cerviello et al 2004) e forse di circa 80 mg di lovastatina . Questi dati hanno portato molti Autori a pensare come l’azione del Monascus purpuerus non sia riconducibile a quella della sola lovastatina ipotizzando piuttosto una sinergia tra le differenti componenti dello stesso. Un ruolo non secondario potrebbe essere giocato dal ruolo di sostanze ad azione antiossidanti. I farmaci ipolipidemizzanti oggi impiegati, statine e fibrati, sembrano avere in questo il limite maggiore: le statine hanno infatti scarsa azione antiossidante e in particolare portano alla deplezione di importanti sostanze antiossidanti endogene come l’ubiquinone (coenzima Q10) (Mortensen et al 1997). Lo stesso effetto hanno i fibrati (Aberg F et al 1998): entrambe le sostanze sembrano in realtà più contribuire a una deplezione delle difese antiossidanti del nostro organismo. Il Coenzima Q in particolare è un coenzima chiave nella catena respiratoria mitocondriale . Livelli bassi di coenzima Q sono sintomo e causa allo stesso tempo di disfunzione mitocondriale , che in genere si traduce in uno squilibrio energetico della cellula che si manifesta con un accumulo di piruvato/lattato (De Pineux et al 1996). Questo non accade con il Monascus purpureus: probabilmente tale effetto è dovuto in parte alla inibizione minore sulla sintesi dell’ubiquinone dovuta alla bassa concentrazione di lovastatina presente nel Monascus e dall’altro probabilmente ad una azione di “risparmio” sul consumo di coenzima Q grazie all’azione parallela di altre sostanze antiossidanti. Forse proprio la deplezione di coenzima Q e il conseguente aumento citoplasmatico di piruvato/lattato è responsabile della tossicità delle statine sulle cellule muscolari (rabdomiolisi) e questo spiegherebbe la relativa assenza di tossicità di questo tipo con Monascus purpureus . Fino ad oggi solamente un caso di modesta rabdomiolisi asintomatica è stato descritto in consumatori di Monascus purpureus e si trattava di un soggetto trapiantato renale in terapia con ciclosporina , agente che notoriamente aumenta la citotossicità di moltissimi rimedi attraverso una forte inibizione del sistema enzimatico CYP3A4 del fegato (…).
Partendo da queste premesse e dal fatto che l’azione del Monascus purpureus risuta da un insieme di azioni non riconducibili alla sola lovastatina recentemente è stato brevettato a livello internazionale un prodotto italiano a base di Monascus, chiamato Lipolysar. In pratica sono stati selezionati ceppi di questo fungo con bassissimo contenuto di lovastatina (2.16 mg di lovastatina) che possiede un effetto ipocolesterolemizzantie e ipoglicemizzante paragonabile a dosi medie di lovastatina (40 mg circa). . In pratica il ragionamento è stato semplice. Se il fungo viene coltivato in vitro e la sua composizione dipende dal terreno di cultura è ovvio che cambiando il terreno è possibile cambiare le sostanze chimiche contenute nel fungo e quindi la sua attività . Potenziando i componenti secondari e diminuendo la concentrazione di lovastatina è stato possibile selezionare ceppi e formulazioni, che con un contenuto bassissimo di lovastatina esercitano la stessa azione ipocolesterolemizzante corrispondente alle dosi maggiori di questa sostanza associata di volta in volta a una maggiore azione ipotriglicerimizzante (da -31% a -43%), a una maggior azione antinfiammatoria sull’endotelio (misurabile sull’attività della Proteina C-reattiva a alta sensibilità , sul Tumor Necrosis Factor-α e sui livelli di Lp(a)) o enfatizzando l’azione ipoglicemizzante o ipotensiva del fungo stesso.
Queste ultime applicazioni sono la dimostrazione di come l’azione degli estratti di Monascus purpureus non possa essere ricondotta alla sola lovastatina e di come l’utilizzo degli estratti in toto di Monascus purpureus possa presentare ancora dei vantaggi rispetto all’impiego delle singole sostanze in esso contenute. Questo ci riporta a due questione tipiche per chi si occupa di estratti vegetali. Da un lato l’azione “in toto” degli estratti spesso dovuta a una interazione dinamica tra le diverse componenti che può assumere le caratteristiche di interazione sinergica o antagonista a seconda della composizione degli stessi. E dall’altro riapre la questione di quanto la filosofia della moderna ricerca farmaceutica, che con il suo interesse focalizzato sull’isolamento di singole molecole rischia di trascurare proprio importanti effetti delle sostanze naturali. Il caso del Monascus ne è esempio tipico: il riaccendersi di ricerche su questo fungo negli ultimi anni ci dimostra che l’antico rimedio cinese possa ancora, grazie alla sinergia dei suoi componenti, offrire interessanti applicazioni all’uomo moderno e forse alla lunga risultare anche più competitivo della sostanza che ne ha determinato la notorietà, della lovastatina.

Zea Universe è lieta di presentare LIPODRENAL il nuovo Trattamento

Conosci la tua età metabolica? O meglio sai che differenza

La FARFALLA simbolo dell’effimero e della resilienza: un variopinto mandala ricco
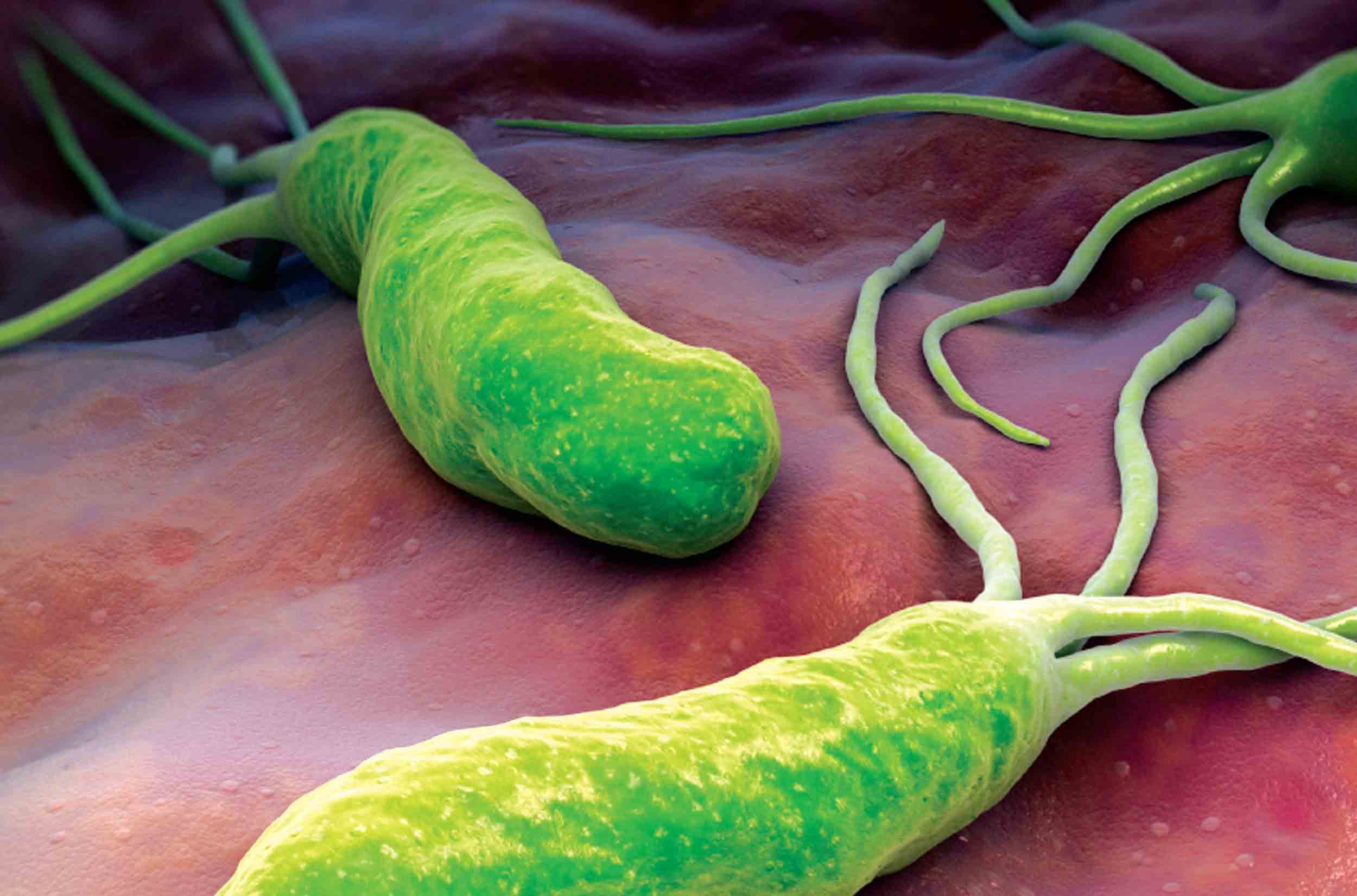
CARATTERISTICHE, SINTOMI E POSSIBILI EFFETTI Il batterio Helicobacter pylori è

Donne e benessere: un matrimonio perfetto. ZEA UNIVERSE è gestita

Lo yoga, una disciplina ecologica Quando affermiamo che lo yoga

I disturbi dissociativi consistono nella perdita dell’integrazione normale dei propri ricordi,

Le piante del solstizio d’estate, alchimia, magia, ricette e sogni
© Zea Universe | ZEA UNIVERSE s.r.l PIVA 06429201004